过氧化氢制取氧气(过氧化氢制取氧气的化学方程式)
2023-05-21 10:06:57 来源: 评论:0 点击:
过氧化氢制取氧气的化学方程式
过氧化氢制取氧气的化学方程式:2H?O?(MnO?催化剂)=2H?O+O?↑
过氧化氢:化学式为H?O?,其水溶液俗称双氧水,外观为无色透明液体,是一种强氧化剂。过氧化氢在常温可以发生分解反应生成氧气和水(缓慢分解),在加热或者加入催化剂后能加快反应,催化剂有:二氧化锰、硫酸铜、碘化氢、二氧化铅、三氯化铁、氧化铁,及生物体内的过氧化氢酶等。
扩展资料:
纯过氧化氢是淡蓝色的粘稠液体,熔点-0.43°C,沸点150.2°C,纯的过氧化氢其分子构型会改变,所以熔沸点也会发生变化。凝固点时固体密度为1.71g/cm3,密度随温度升高而减小。它的缔合程度比H?O大,所以它的介电常数和沸点比水高。
碱性过氧化氢制法:生产碱性过氧化氢用含醌空气电极,其特征在于每对电极由阳极板、塑料网、阳离子隔膜和含醌空气阴极组成。
在电极工作区的上、下端设有进入流体的分配室和排出流体的收集室,在流体进口处设有节流孔,多组元电极采用有限制的偶极串联接法,加长阳极循环碱水进、出口用的塑料软管后再接至集液总管,多组元电极组由单元极板组装。
过氧化氢,它的分子是由2个氢原子和2个氧原子组成的,在常温下能少量分离出氧气,在加入二氧化锰的情况下能剧烈反应,分解出大量的氧气,中学化学实验室常用这种方式制取氧气。
问过氧化氢制取氧气的实验
1.检查气密性:1)组装好后向分液漏斗中加少量水~当水到分液漏斗下口时,看水是否继续下流。下流为没密封。2)关闭分液漏斗,将出气口一端放如水中~微热试管~另一段有均匀气泡冒出则密封良好。(不能检查分液漏斗的塞是不是密封的,不提倡)
2.当然是检查完后加二氧化锰了,把塞子拿下来后,用药勺取少量二氧化锰加入。
3.1)可以一边制取一边加入过氧化氢(防止浓度降低造成出氧慢)。2)保持气密性。
4.为什么检查气密性的时候漏斗没过水就不能往下流了?这其中原理什么的是怎么回事?
答:当没没过水时~试管内气体可以从分液漏斗溢出,当没过管口时,达到水封了~要是试管气密性良好的话就不能有水流下了~因为试管的气压和外界气压相等了~
5.分液漏斗为什么要完全没入水中?
答:应该是分液漏斗的端口完全没入水中~要不没入水中制取的氧气就会从分液漏斗溢出。
6.因为后加固体要开塞的。这个反应是很快的~你要开塞就让氧气跑走了~
7.此反应是比较剧烈的反应~所以不推荐用长颈漏斗~防止液体从长颈漏斗喷出~
8.高锰酸钾,氯酸钾和过氧化氢制取氧气的原理是什么?
答:2KMnO4---K2MnO4+MnO2+O2
氯酸钾的我忘了。(要是方便的话给我它的化学式吧)
2H2O2---2H2O+O2.3者都是分解反应。
实验过程
1.检验气密性
2.装二氧化锰
3.将出气端放入水中
4.加双氧水
5.当气泡均匀出来时,用烧瓶用向下排气法接受氧气
资料部分展示



知识点一氧气的实验室制法
一、加热高锰酸钾制取氧气
1.药品:高锰酸钾(暗紫色固体,化学式:KMnO4)。
2.反应原理
高锰酸钾
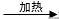
锰酸钾+ 二氧化锰 + 氧气
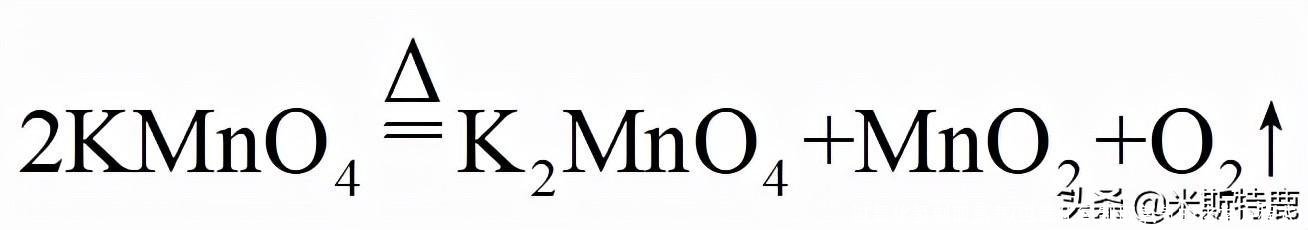
3.实验装置
【问题1】给试管中固体加热应如何操作?为什么?
【问题2】用向上排空气法收集的气体应具备什么性质?
【问题3】用向下排空气法收集的气体应具备什么性质?
【问题4】用排水法收集的气体应具备什么性质?
【小结】

【KMnO4制氧气的制取装置】
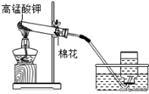
4.实验步骤
①连接仪器,检查装置的气密性。
②将药品平铺在试管底部,在试管口放一小团棉花,用带导管的单孔橡皮塞塞紧试管口。
③将试管固定在铁架台上。将集气瓶装满水,并用玻璃片盖住瓶口(注意不能有气泡),然后把盛满水的集气瓶连同玻璃片一起倒立在盛水的水槽内。
④点燃酒精灯,加热试管。
⑤当导管口有连续均匀的气泡放出时将导管伸入集气瓶口开始收集。当集气瓶口有气泡冒出时表明瓶内已经集满氧气,在水面下用玻璃片盖住瓶口,小心地把集气瓶移出水槽,正放在桌面上。
⑥将导管撤离水槽。
⑦熄灭酒精灯,停止加热。
5.实验反思
【问题1】导管刚刚露出橡皮塞即可,为什么?
【问题2】为什么要在试管口塞一团棉花?
【问题3】为什么等气泡连续均匀冒出时,开始收集气体?
【问题4】用排水法收集氧气时,怎样证明集气瓶中已收集满氧气?
【问题5】用向上排空气法收集氧气时,怎样证明集气瓶中已收集满氧气?
【问题6】用排水法收集完毕时,为什么要先从水中取出导管再停止加热?
【问题7】如何检验收集到的气体是否为氧气?
二、加热氯酸钾制取氧气
1.药品
氯酸钾(白色固体,化学式:KClO3)、二氧化锰(黑色粉末,化学式:MnO2)。
2.反应原理
氯酸钾

氯化钾+ 氧气

3.实验装置
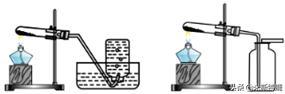
三、过氧化氢溶液制取氧气
1.药品
过氧化氢溶液(无色溶液,化学式:H2O2)、二氧化锰(黑色粉末,化学式:MnO2)。
2.反应原理
过氧化氢
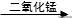
水+ 氧气
3.实验装置
【发生装置】
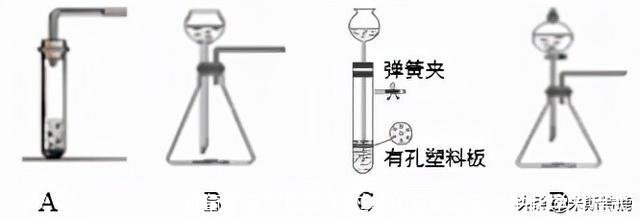
各发生装置优点:A、最简易的装置,操作简单;B、可以随时添加药品(长颈漏斗的下端管口应伸入液面以下);C、可以随时控制反应的发生和停止;D、可以随时控制反应速率。
【收集装置】

4.万能瓶使用
装置正放 | 排空气法收集气体 | 密度比空气密度大 | 长进短出 |
密度比空气密度小 | 短进长出 | ||
排水法收集气体时(与密度无关) | 短进长出 | ||
装置倒放 | 排空气法收集气体 | 密度比空气密度大 | 短进长出 |
密度比空气密度小 | 长进短出 | ||
排水法收集气体时(与密度无关) | 长进短出 | ||
5.实验步骤
①连接仪器,检查装置的气密性。
②装药品:先向锥形瓶内加入二氧化锰固体,塞好双孔橡皮塞,向长颈漏斗中加入过氧化氢溶液。
③收集气体。

1.实验室用 KMnO4制氧气并验证氧气的性质,下列操作正确的是( )
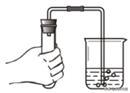
A.检査装置气密性
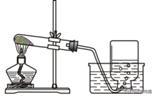
B.加热KMnO4制O2
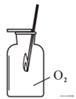
C.验证O2已集满
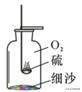
D.硫在O2中燃烧
【答案】A
【解析】A、检査装置气密性方法是把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气,故A正确;B、高锰酸钾是粉末状的,为防止高锰酸钾进入导管,要在试管口塞一团棉花,故B不正确;C、氧气的验满,带火星的木条要放在集气瓶口,木条复燃,说明已收集满,故C不正确;D、硫在氧气中点燃生成二氧化硫,二氧化硫和水反应,则硫在O2中燃烧集气瓶底部要加入水,故D不正确。故选A。
2.关于“加热高锰酸钾制得氧气并用排水法收集”的实验,下列说法正确的是( )
A.制取气体时,先装药品,然后检验装置的气密性
B.反应结束时,先停止加热,然后将导管移出水面
C.导气管口开始产生气泡时,立即用装满水的集气瓶收集气体
D.装有高锰酸钾的试管口要放一小团棉花,目的是防止反应时药品进入导气管
【答案】D
【解析】A、制取气体时,先检验装置的气密性,后添加药品,A错;B、反应结束时,先将导管移出水面,后停止加热,防止水倒吸入试管,试管炸裂,B错;C、导气管口有连续均匀气泡时,开始用装满水的集气瓶收集气体,C错;D、装有高锰酸钾的试管口要放一小团棉花,目的是防止反应时药品进入导气管,D正确。故选D。
3.根据下图回答问题:
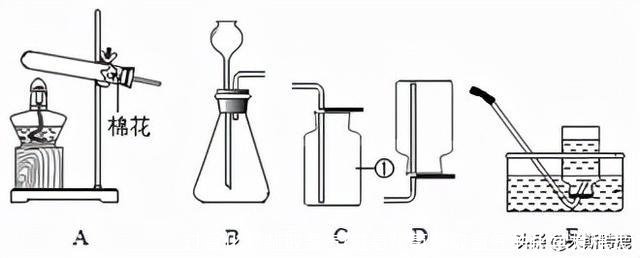
(1)写出仪器①的名称:_________________。
(2)实验室若用装置A制取较纯净的氧气,反应的化学方程式为______________,可以选______________(填装置序号)作收集装置。
(3)实验室制取CO2,应选择的发生和收集装置的组合是_____________(填装置序号)。在装入药品前,必须要进行的实验操作是______________。
【答案】(1)集气瓶;
(2)
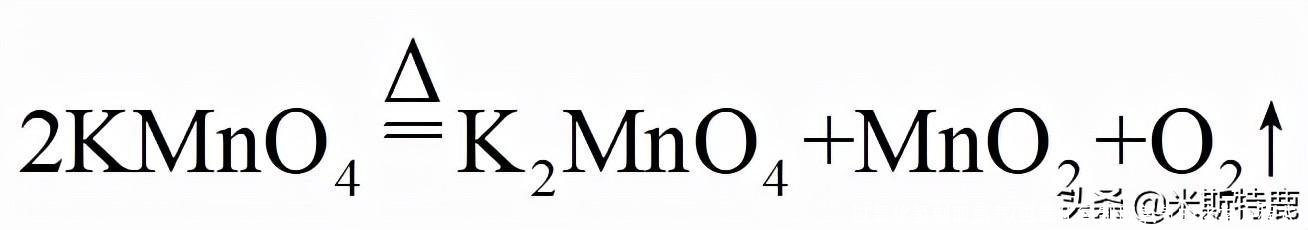
;E ;(3)BC;检查装置的气密性
【解析】(1)由图可知,仪器①的名称是:集气瓶;(2)装置A适用于固体加热反应制取气体,且试管口有一团棉花,适用于加热高锰酸钾制取氧气,高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,该反应的化学方程式为:;氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,排水法收集的氧气比较纯净,故收集装置选E;(3)实验室通常用石灰石和稀盐酸反应制取二氧化碳,该反应属于固液不加热反应,发生装置应选B,二氧化碳溶于水,且密度比空气大,应用向上排空气法收集,收集装置应选C,故应选择的发生和收集装置的组合是BC;在装入药品前,必须要进行的实验操作是:检查装置的气密性,防止收集不到气体。
4.化学是一门以实验为基础的科学。根据下列图示回答问题。
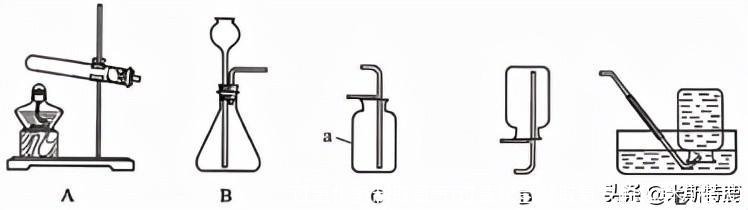
①仪器a的名称是_________。
②实验室用高锰酸钾制取氧气的化学反应方程式为_______。所选用的发生装置是______(填序号)。若用E装置收集氧气,实验完毕后,先将导管从水槽中移出,再熄灭酒精灯的目的是_________。
③氢气是一种清洁能源。实验室常用锌粒和稀硫酸来制取氢气,应选择的发生装置是_____(填序号,下同),收集装置除选E外,还可以选_________。
【答案】(1)集气瓶;(2
)
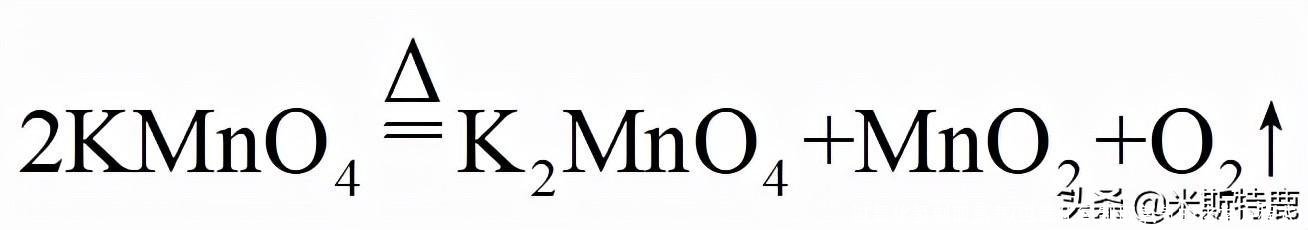
;A;防止水倒流,使试管炸裂;(3)B ;D
【解析】①据图可知仪器a的名称是集气瓶;②如果用高锰酸钾制氧气就需要加热,所选用的发生装置是A,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,化学反应方程式为;若用E装置收集氧气,实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;③用锌粒和稀硫酸在常温下制取氢气的发生装置为固液常温型,故选装置B;氢气是一种无色无味,溶于水,相同条件下密度比空气小的气体,选择收集装置为:D或E。

1.下列实验用常用于实验室制取气体,回答下列问题:
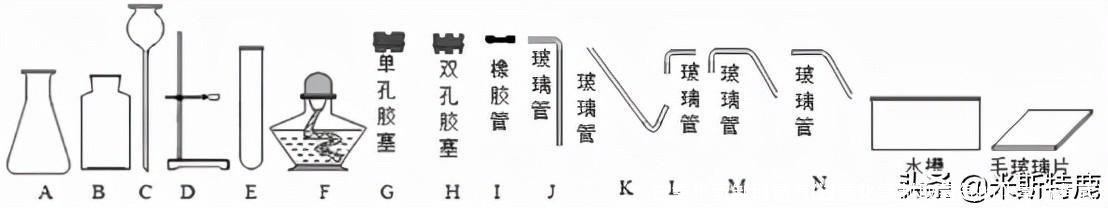
(1)仪器E的名称是____________________;
(2
)用
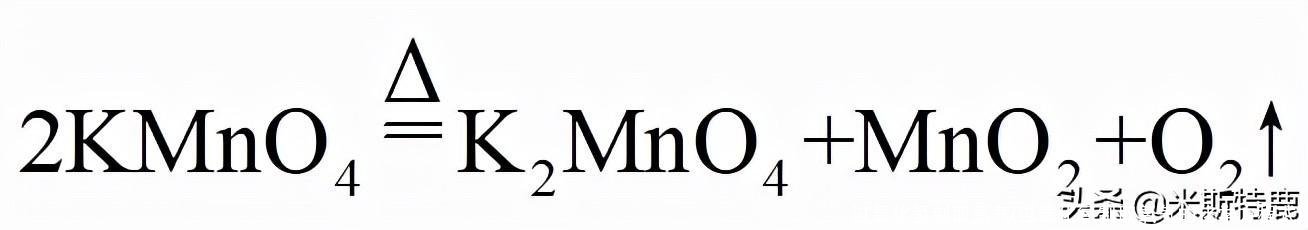
来制取O2,并用排水法收集,组装制取装置时,除选用上图中的B、D、E、G、I、K、N、P外,还必须选用图中的__________________。
【答案】(1)试管;(2)F、O ;
【解析】(1)通过观察可知仪器E的名称是试管;(2)用加热高锰酸钾的方法来制取氧气需要有热源,酒精灯F,用排水法来收集氧气需要有水槽O。
2.如图是实验室常用的实验装置,请回答下列问题。
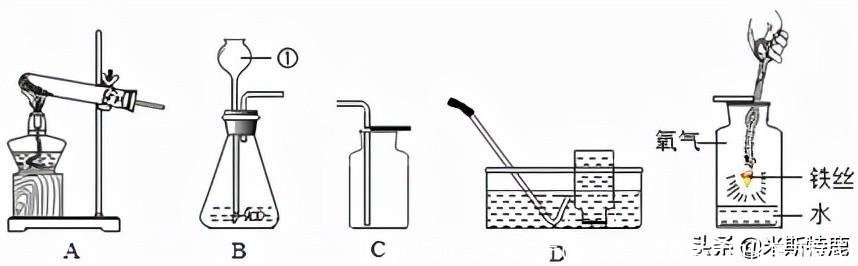
(1)仪器①的名称_____。
(2)用A装置制取氧气的化学方程式_______________。C和D都可以收集O2,选择D装置的优点_____。
(3)E装置中水的作用_____。
【答案】(1)长颈漏斗;(2
)
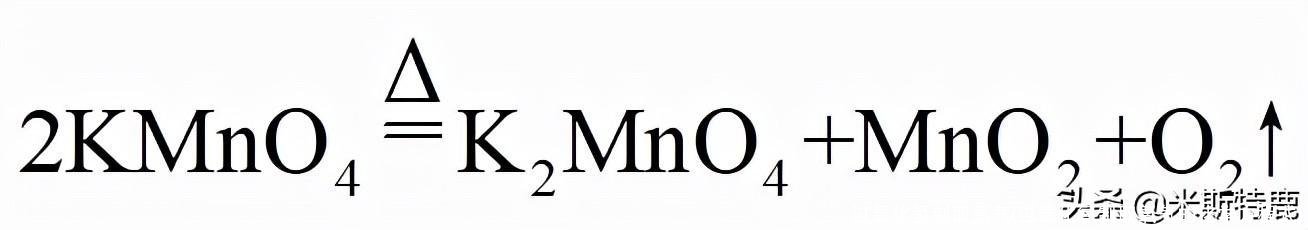
;收集的气体较为纯净;(3)防止生成物熔化溅落下来使瓶底炸裂
【解析】解:(1)仪器①的名称是长颈漏斗;(2)装置A属于固体加热型,试管口放有一团棉花,采用的加热高锰酸钾的方法,高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是。C和D都可以收集O2,D装置是排水法,选择D装置的优点是收集的气体较为纯净;(3)铁丝在氧气中燃烧时,为防止生成物熔化溅落下来使瓶底炸裂,集气瓶的底部应放少量的水或铺一层细沙,E装置中水的作用是防止生成物熔化溅落下来使瓶底炸裂。故答案为:(1)长颈漏斗;(2);收集的气体较为纯净;(3)防止生成物熔化溅落下来使瓶底炸裂。
3.根据下列装置图回答问题:
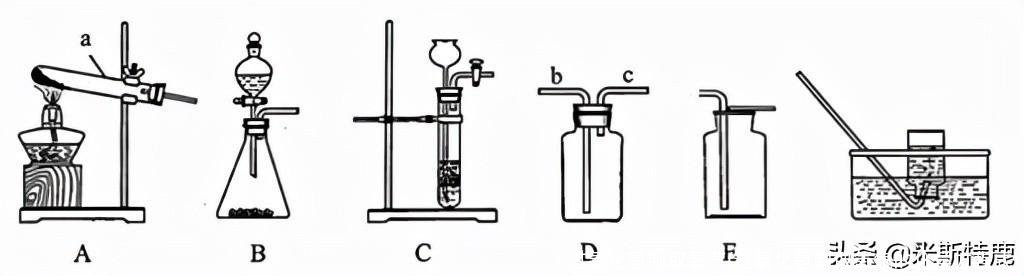
(1)仪器a的名称是_______________。
(2)用氯酸钾和MnO2制取较纯净的O2时,应选择的装置是___________(填标号),化学方程式是____________,若用向上排空气法收集氧气,验满的方法是__________________。
(3)碳酸钙粉末与稀硫酸反应可制得CO2,化学方程式是__________________。
(4)实验室制取H2时,通过控制液体流速,从而得到平稳气流,选择的发生装置是______________(填标号),若用排水法收集H2,应从D装置的____________(填“b”或“c”)口通入气体。
【答案】试管 A

将带火星的小木条平放到集气瓶口,若小木条复燃,则满 B c
【解析】(1)仪器a的名称是试管;(2)用氯酸钾和MnO2制取较纯净的O2时,属于固体混合加热型,应选择的装置是A,加热条件下,二氧化锰催化氯酸钾反应生成氯化钾和氧气,反应的化学方程式是 ,若用向上排空气法收集氧气,验满的方法是将带火星的小木条平放到集气瓶口,若小木条复燃,则满;(3)碳酸钙粉末与稀硫酸反应可制得二氧化碳和磷酸钙,化学方程式是 ;(4)实验室制取氢气时,通过控制液体流速,从而得到平稳气流,选择的发生装置是B,通过分液漏斗控制液体的添加量,可得到稳定的气流,若用排水法收集氢气,应从D装置的c口通入气体,将水从b口排出。
4.利用下列装置进行气体的制取实验,请问答下列问题:
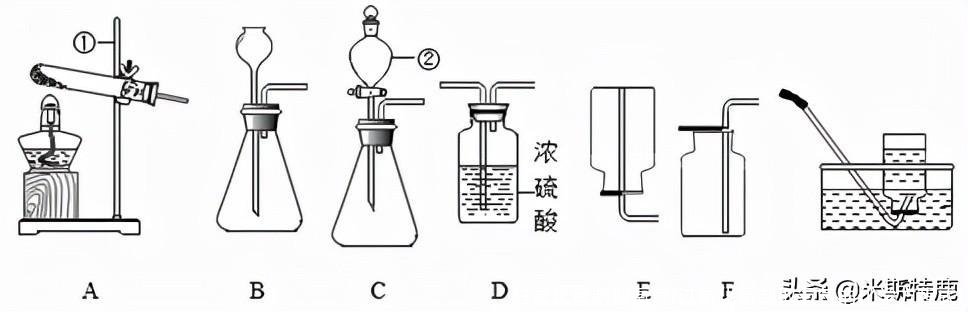
(1)写出仪器的名称:①____________②______________。
(2)实验室用过氧化氯溶液制取氧气时,若要制取一瓶干燥的氧气,必须使气体通过__________(填字母,下同)装置,选用装置___________收集,验满的方法是____________。
(3)实验室用加热高锰酸钾固体的方法制取较纯净的氧气,选用发生装置____________和收集装置G组合,检查该装置气密性的方法是:连接好仪器,把导管的一端浸入水中,_____________,证明装置连接完好、不漏气。
(4)实验室用电石固体与饱和食盐水常温下反应制取乙炔(C2H2)气体,同时有糊状 Ca(OH)2生成,发生装置选用C而不选用B的原因是_____________;乙炔充分燃烧的化学方程式为____________。
【答案】(1)①铁架台;②分液漏斗;(2)D ; F;用带火星的木条靠近集气瓶口,若木条复燃,则已经充满;(3)A;手紧握试管,如果导管口有气泡冒出;(4)可以控制滴加液体速率和防止糊状Ca(OH)2堵塞长颈漏斗的下端;
【解析】(1)由图可知,仪器①的名称是:铁架台;仪器②的名称是:分液漏斗;(2)浓硫酸具有吸水性,且浓硫酸与氧气不反应,可用浓硫酸干燥氧气,故若要制取一瓶干燥的氧气,必须使气体通过D装置;
氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,要想得到干燥的氧气,应用向上排空气法收集,故收集装置选F;氧气具有助燃性,氧气验满:用带火星的木条靠近集气瓶口,若木条复燃,则已经充满;(3)高锰酸钾加热制取氧气,属于固体加热反应,发生装置应选A;检查该装置气密性的方法是:连接好仪器,把导管的一端浸入水中,手紧握试管,如果导管口有气泡冒出,证明装置连接完好、不漏气;(4)发生装置选用C而不选用B,因为C装置可通过分液漏斗控制药品的滴加速率,从而控制反应速率,同时分液漏斗下端无需浸入液面以下,糊状Ca(OH)2不会堵塞漏斗的下端,故填:可以控制滴加液体速率和防止糊状Ca(OH)2堵塞长颈漏斗的下端;乙炔充分燃烧生成二氧化碳和水,该反应的化学方程式为:。
5.实验室制取气体时需要的一些装置如下图所示,请回答下列问题。
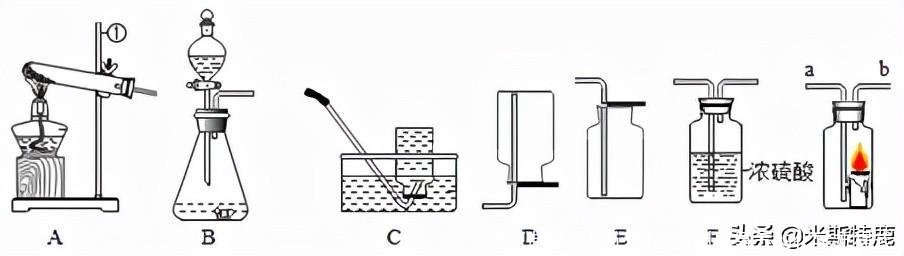
(1)写出仪器①的名称__________________。
(2)实验室用A装置制取并收集干燥的氧气,所选装置的连接顺序为:A→________→________(填装置代号),写出A装置中使用催化剂制取氧气的化学方程式:________________________。若用C装置收集氧气,导管口开始有气泡放出时,不宜立即收集,应在________________时,开始收集气体。
(3)某兴趣小组的同学在实验室连接B、G装置进行实验。若实验时,在G装置中放置一个燃着的蜡烛,实验过程中蜡烛熄灭,说明生成的气体具有_________________的化学性质,则B装置中反应的化学方程式为________________________;若将G装置中的蜡烛取出来,改用G装置收集此气体时,验满的方法是_____________________。
【答案】(1)铁架台;(2)F;E ;

;导管口气泡连续均匀冒出;(3)不可燃、不助燃;CaCO3+2HCl=CaCl2+H2O+CO2↑;将燃着的木条放在b管口处,若木条火焰熄灭,则集满二氧化碳
【解析】(1)根据图示,仪器①的名称是:铁架台;(2)实验室用A装置制取并收集干燥的氧气,制取后,应先用盛有浓硫酸的F装置干燥,再用向上排空气法收集,所选装置的连接顺序为:A→F→E;A装置中使用催化剂制取氧气,对应的是利用氯酸钾和二氧化锰的混合物加热制取氧气,化学方程式是:。若用C装置收集氧气,导管口开始有气泡放出时,不宜立即收集,因为开始排出的气体是装置中原有的空气,所以应在导管口气泡连续均匀冒出时,开始收集气体。(3)在实验室连接B、G装置进行实验。若实验时,在G装置中放置一个燃着的蜡烛,实验过程中蜡烛熄灭,说明B装置中生成的气体具有不可燃、不助燃的化学性质;在初中阶段利用B装置生成的不可燃、不助燃的气体是二氧化碳,反应物是大理石和稀盐酸,大理石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成二氧化碳、水、氯化钙,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;若将G装置中的蜡烛取出来,改用G装置收集二氧化碳,由于二氧化碳的密度比空气的大,气体应从a管进入,瓶内的空气从b管排出,验满的方法是:将燃着的木条放在管口b处,若木条火焰熄灭,则集满二氧化碳。
Q版化学
[Q版化学】一位不安分的化学老师的公众号!让化学学习变得不再困难,趣味学习化学,志在打破传统教学的枯燥无味!
公众号

大鹿化学工作室
视频号

大鹿化学工作室
视频号

大鹿化学工作室
视频号
相关热词搜索: